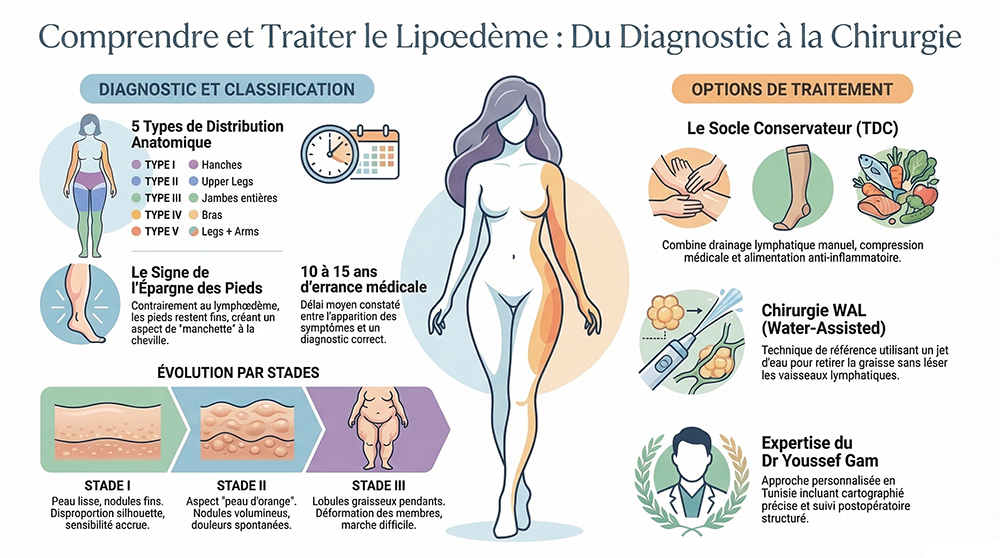
Lipœdème : types, zones et traitements
Le lipœdème est une pathologie du tissu adipeux aux manifestations cliniques variables, dont la prise en charge nécessite une cartographie précise des zones atteintes et une compréhension fine des sous-types anatomiques. Loin d’être une entité uniforme, le lipœdème se décline en cinq types topographiques distincts — chacun avec ses caractéristiques propres, son évolution et ses implications thérapeutiques — et en quatre stades d’évolution croissante. Cet article propose une description exhaustive de la classification du lipœdème par types et zones anatomiques, passe en revue les stratégies thérapeutiques disponibles de la prise en charge conservative à la chirurgie spécialisée, et présente l’expertise du Dr Youssef Gam en Tunisie comme référence francophone pour le traitement chirurgical.
1. Introduction : une maladie polymorphe et sous-diagnostiquée
Le lipœdème — du grec lipos (graisse) et oídema (gonflement) — est une maladie systémique du tissu adipeux décrite pour la première fois par Allen et Hines en 1940 à la Mayo Clinic [1]. Près de 85 ans plus tard, malgré une prévalence estimée à 10-18 % des femmes adultes dans les pays occidentaux, le lipœdème reste l’une des maladies chroniques les plus méconnues et les plus mal diagnostiquées de la médecine moderne — le délai moyen entre l’apparition des premiers symptômes et l’établissement d’un diagnostic correct étant encore estimé à 10-15 ans dans plusieurs pays européens [2].
Cette méconnaissance s’explique en partie par la diversité des présentations cliniques du lipœdème. Contrairement à une représentation simpliste qui le réduit à de « grosses jambes », le lipœdème se présente sous plusieurs formes topographiques distinctes, pouvant toucher les cuisses, les genoux, les mollets, les chevilles, les bras — ou plusieurs de ces zones simultanément — selon un pattern de distribution caractéristique propre à chaque patiente. Cette diversité implique que la prise en charge thérapeutique ne peut être standardisée : elle doit être personnalisée en fonction du type de lipœdème, du stade évolutif et des zones anatomiques concernées.
Cet article a pour objectif de fournir aux patients et aux professionnels de santé une cartographie clinique complète du lipœdème — classification par types et zones, description des stades évolutifs, diagnostic différentiel — assortie d’une revue des stratégies thérapeutiques disponibles, de la prise en charge conservative à la chirurgie WAL spécialisée.
2. Classification du lipœdème par types anatomiques
La classification la plus utilisée en pratique clinique est celle proposée par Herbst et al. (2012), qui distingue cinq types topographiques selon la localisation anatomique des dépôts adipeux pathologiques [3]. Cette classification conditionne directement le plan thérapeutique, notamment la séquence et l’étendue des zones à traiter par liposuccion WAL.
2.1 Type I — Atteinte des hanches et fesses
Le type I est le plus précoce dans l’histoire naturelle de la maladie. Il se manifeste par une accumulation symétrique de tissu adipeux pathologique dans la région des hanches, des fesses et du haut des cuisses (région glutéale et trochantérienne), réalisant une morphologie dite « en culotte de cheval » ou « en selle ». Les membres inférieurs conservent un aspect relativement normal en dessous du genou à ce stade précoce [4].
Ce type est souvent le premier à apparaître à la puberté et peut pendant de nombreuses années être le seul territoire affecté, avant que la maladie ne progresse vers les types II ou III. Le type I pur — limité à la zone trochantérienne — est celui qui bénéficie le plus rapidement d’une liposuccion WAL ciblée, les résultats fonctionnels et esthétiques étant généralement très satisfaisants dès la première session chirurgicale.
2.2 Type II — Atteinte des hanches aux genoux
Le type II est défini par une extension de l’atteinte des hanches jusqu’aux genoux, incluant la face interne et externe des cuisses, avec formation caractéristique d’un bourrelet adipeux médial au niveau du genou (signe du « coussin du genou » ou knee pad). Ce bourrelet interne du genou est l’un des signes cliniques les plus caractéristiques et les plus reconnaissables du lipœdème de type II [5].
La face interne des cuisses et la région du genou sont des zones particulièrement douloureuses à la palpation. La formation de ce bourrelet médial peut gêner significativement la marche normale et contribuer à une hyperstatique en valgus du genou, source de douleurs articulaires surajoutées à long terme. Le type II représente la présentation la plus fréquemment rencontrée en consultation spécialisée.
2.3 Type III — Atteinte des hanches aux chevilles
Le type III correspond à une extension de l’atteinte sur l’ensemble des membres inférieurs, depuis les hanches jusqu’aux chevilles, respectant strictement les pieds — le signe de l’épargne des pieds (ou « manchette ») constituant l’un des éléments diagnostiques pathognomoniques du lipœdème. Le passage abrupt entre la cheville atteinte et le pied normal donne un aspect caractéristique en « bottes » ou « guêtres » [6].
À ce stade, l’atteinte est généralement circumférentielle, touchant aussi bien la face antérieure que postérieure et les faces latérales des jambes. Les douleurs spontanées au repos, les ecchymoses faciles et la lourdeur permanente des membres inférieurs sont particulièrement prononcées dans ce type. La prise en charge chirurgicale nécessite plusieurs sessions pour couvrir l’ensemble des zones atteintes.
2.4 Type IV — Atteinte des membres supérieurs
Le type IV se caractérise par l’atteinte des membres supérieurs — bras, avant-bras, voire région des épaules — en plus ou à la place des membres inférieurs. L’accumulation graisseuse pathologique touche préférentiellement la face interne du bras (région brachiale médiale), réalisant un aspect de « bras en ailes » (bat wings) particulièrement gênant pour les mouvements quotidiens et significativement impactant sur l’image corporelle [7].
Le type IV pur (membres supérieurs isolément) est plus rare que les atteintes des membres inférieurs ; il est plus fréquemment associé en pratique à une atteinte concomitante des membres inférieurs (types II ou III + IV). La liposuccion WAL des membres supérieurs nécessite une technique particulièrement précise en raison de la proximité des structures neurovasculaires importantes (nerf médian, artère brachiale).
2.5 Type V — Atteinte des mollets isolée
Le type V, également appelé lipœdème crural isolé, est défini par une atteinte préférentielle des mollets, avec épargne relative des cuisses. Il s’agit d’une présentation plus rare, souvent méconnue car le gonflement symétrique des mollets est facilement attribué à une insuffisance veineuse chronique ou à un lymphœdème bilatéral [8].
La distinction avec l’insuffisance veineuse chronique repose sur l’hypersensibilité cutanée du type V (absente dans l’insuffisance veineuse), les ecchymoses faciles, et la résistance à l’élévation des membres. Le type V répond bien à la liposuccion WAL des mollets, mais exige une technique particulièrement attentive à la préservation du réseau lymphatique superficiel de la région.
3. Stades évolutifs : de la discrétion à l’invalidité
Indépendamment du type topographique, le lipœdème évolue selon quatre stades de sévérité croissante, décrits par Herbst (2012) et universellement utilisés dans la littérature [9]. Ces stades reflètent une progression histologique réelle, de l’hyperplasie adipocytaire simple jusqu’à la fibrose tissulaire extensive et au lipo-lymphœdème des stades avancés.
3.1 Stade I — Hyperplasie adipocytaire débutante
La peau est lisse en apparence, mais le tissu sous-cutané est déjà épaissi, avec de petits nodules fins palpables à l’examen minutieux. Les contours corporels sont modifiés avec une disproportion déjà nette entre le haut et le bas du corps. Les douleurs sont modérées ou absentes au repos, mais la sensibilité à la pression est augmentée. Ce stade est souvent confondu avec une simple « tendance à prendre du poids dans les hanches et les cuisses », retardant le diagnostic de plusieurs années.
3.2 Stade II — Nodularité et irrégularité cutanée
La surface cutanée présente des irrégularités de relief : aspect matelassé, capitonné ou « peau d’orange » sur les zones atteintes. Des nodules plus volumineux — de 1 à plusieurs centimètres — sont palpables dans le tissu sous-cutané, correspondant à des lobules adipeux entourés de fibrose péri-adipocytaire. Les douleurs spontanées apparaissent, majorées à la chaleur ou lors de la station debout prolongée. La grande majorité des patientes consultant un spécialiste pour la première fois se trouvent à ce stade.
3.3 Stade III — Lobules pendants et déformation majeure
Des lobules graisseux volumineux sont visibles et pendent sous l’action de la pesanteur, déformant notablement le galbe des membres. Ces lobules peuvent provoquer des frottements, des irritations cutanées et des difficultés significatives pour s’habiller ou se chausser. Le retentissement fonctionnel est majeur : limitation de la marche, difficultés à monter les escaliers, incapacité à pratiquer la plupart des activités sportives. La douleur est permanente, souvent invalidante, avec un score EVA moyen de 6-8/10. L’indication chirurgicale est généralement formelle à ce stade.
3.4 Stade IV — Lipo-lymphœdème : la complication redoutée
Le stade IV, ou lipo-lymphœdème, correspond à la surcharge du système lymphatique par l’accumulation liquidienne et protéique progressive dans le tissu lipœdémateux. Le signe de Stemmer devient positif, les pieds et les chevilles commencent à être touchés, et des épisodes d’érysipèle ou de lymphangite apparaissent avec une fréquence croissante. À ce stade, la prise en charge est plus complexe, nécessitant une expertise lymphologique spécialisée en complément de la chirurgie.
4. Diagnostic différentiel : ne pas confondre
Le diagnostic du lipœdème est clinique, mais plusieurs pathologies lui ressemblent superficiellement et doivent être systématiquement écartées :
- Obésité gynoïde : la distribution gynoïde de la graisse dans l’obésité commune n’entraîne ni douleur spontanée, ni ecchymoses faciles, ni résistance spécifique à la perte de poids dans les zones affectées sous régime calorique adapté.
- Lymphœdème primaire ou secondaire : touche habituellement les pieds (signe de Stemmer positif), peut être unilatéral, s’améliore significativement avec l’élévation des membres. Absence d’hypersensibilité cutanée et d’ecchymoses spontanées.
- Insuffisance veineuse chronique : œdème déclive, régressif au décubitus, associé à des varices, une dermite ocre, voire des ulcères veineux. L’œdème est mou et indolore à la palpation.
- Lipodystrophie : redistribution pathologique de la masse grasse d’origine génétique, auto-immune ou iatrogène. L’absence de douleur caractéristique et la présence fréquente d’anomalies métaboliques associées orientent le diagnostic.
- Myxœdème hypothyroïdien : rétention liquidienne généralisée, indolore, sans ecchymoses, associée aux signes biologiques de l’hypothyroïdie. Régresse sous traitement par lévothyroxine.
En pratique, le lipœdème et ces pathologies peuvent coexister — notamment le lipo-lymphœdème (association lipœdème + lymphœdème secondaire) ou le lipœdème sur fond d’obésité — ce qui justifie le recours à des examens complémentaires ciblés : échographie des parties molles, lymphoscintigraphie, écho-Doppler veineux des membres inférieurs et bilan hormonal [10].
5. Traitements conservateurs : le socle thérapeutique
5.1 Le traitement décongestif complexe (TDC)
Le traitement décongestif complexe (TDC) constitue le pilier du traitement conservateur du lipœdème, quelle que soit la zone atteinte ou le stade évolutif. Il combine plusieurs composantes complémentaires dont l’efficacité a été démontrée dans la réduction de la douleur, de l’œdème et du retentissement fonctionnel [11] :
- Drainage lymphatique manuel (DLM) : technique de massage doux codifiée, visant à stimuler la contractilité des collecteurs lymphatiques et à favoriser la résorption du liquide interstitiel. Réalisé par un kinésithérapeute spécialisé en lymphologie, à raison de 2 à 5 séances hebdomadaires en phase intensive.
- Compression médicale : port de bas, collants ou manchons de compression médicale (classe II ou III), sur mesure dans les cas sévères, dès le lever. La compression doit être adaptée spécifiquement à la zone atteinte (membres inférieurs, membres supérieurs).
- Pressothérapie pneumatique séquentielle : compression mécanique progressive par manchons pneumatiques gonflables, utilisable à domicile en complément du DLM en cabinet. Particulièrement utile pour les stades II et III.
- Exercice physique adapté (EPA) : activités à faible impact articulaire privilégiées — natation, aquagym, vélo stationnaire, marche nordique, yoga. L’exercice améliore le retour lymphatique et veineux, réduit l’inflammation systémique et améliore significativement la qualité de vie.
5.2 Approche nutritionnelle anti-inflammatoire
L’alimentation ne peut éliminer le tissu adipeux lipœdémateux, mais une stratégie nutritionnelle anti-inflammatoire peut réduire les marqueurs biologiques d’inflammation, diminuer la douleur et améliorer la composition corporelle globale. Deux approches sont soutenues par la littérature [12] :
- Régime cétogène ou très faible en glucides (LCHF) : plusieurs études pilotes (2019-2024) rapportent une réduction significative des douleurs et une amélioration de la qualité de vie. L’effet passe probablement par la réduction de l’hyperinsulinémie et les propriétés anti-inflammatoires des corps cétoniques.
- Régime méditerranéen : alternative bien tolérée et nutritionnellement équilibrée, riche en acides gras oméga-3, polyphénols et fibres fermentescibles. Améliore la sensibilité à l’insuline et réduit les marqueurs inflammatoires circulants.
Dans tous les cas, une hydratation adéquate (1,5 à 2 litres d’eau par jour) est indispensable au maintien de la fonction lymphatique et à la fluidité du liquide interstitiel.
5.3 Traitements pharmacologiques complémentaires
Plusieurs classes de médicaments peuvent être utilisées en complément du TDC :
- Veinotoniques et flavonoïdes (diosmine, rutine, hespéridine) : améliorent la résistance capillaire et réduisent la perméabilité microvasculaire, contribuant à diminuer la rétention liquidienne interstitielle.
- Anti-inflammatoires non stéroïdiens (AINS) : utilisés ponctuellement pour les poussées douloureuses aiguës ; leur usage chronique est déconseillé.
- Semaglutide et agonistes GLP-1 : données préliminaires (2023-2025) suggérant un bénéfice sur la composante inflammatoire et la douleur chez les patientes avec résistance à l’insuline associée [13].
- Naltrexone à faible dose (LDN) : données préliminaires encourageantes sur la modulation de l’inflammation et de la douleur dans le lipœdème ; essais cliniques en cours.
6. La chirurgie WAL : le traitement de référence par type et par zone
6.1 Principe et spécificités de la liposuccion WAL dans le lipœdème
La liposuccion par vibro-aspiration assistée à l’eau (Water-Assisted Liposuction, WAL) est aujourd’hui considérée comme le traitement chirurgical de référence du lipœdème [14]. Contrairement à la liposuccion esthétique standard, la WAL emploie un jet d’eau finement contrôlé pour décoller délicatement les adipocytes de leur stroma conjonctif et vasculo-lymphatique, préservant ainsi l’intégrité des vaisseaux lymphatiques.
Cette préservation lymphatique est fondamentale dans le lipœdème : le système lymphatique des zones atteintes est déjà fragilisé et toute lésion supplémentaire pourrait précipiter l’évolution vers un lipo-lymphœdème iatrogène. La WAL permet d’obtenir des résultats durables en termes de réduction du volume et de la douleur, avec un profil de sécurité bien documenté dans les grandes séries publiées [15].
6.2 Stratégie chirurgicale selon le type de lipœdème
La planification chirurgicale doit être adaptée au type de lipœdème, avec une séquence logique des zones à traiter en priorité :
- Type I (hanches/fesses) : traitement des régions trochantériennes, fessières et hanche en une ou deux sessions. Résultats fonctionnels et esthétiques généralement excellents dès la première intervention.
- Type II (hanches aux genoux) : traitement en deux phases, en séparant idéalement l’intervention sur les cuisses et celle sur le bourrelet médial du genou. Ce bourrelet requiert une technique particulièrement précise pour éviter toute lésion du réseau lymphatique poplité.
- Type III (hanches aux chevilles) : prise en charge progressive en trois à quatre sessions chirurgicales espacées de 3 à 6 mois, traitant successivement les cuisses, les genoux, les mollets et les chevilles.
- Type IV (membres supérieurs) : liposuccion WAL de la face interne du bras et, si nécessaire, de l’avant-bras. La technique exige une maîtrise chirurgicale particulière en raison de la présence des structures neurovasculaires du bras.
- Type V (mollets isolés) : traitement ciblé des mollets en une ou deux sessions, avec préservation méticuleuse du réseau lymphatique superficiel et attention particulière aux structures anatomiques de la loge postérieure.
6.3 Résultats à long terme et limites
Les données à long terme (5-10 ans) sur la liposuccion WAL dans le lipœdème montrent des résultats globalement très favorables : 80 à 90 % des patientes rapportent une réduction durable des douleurs, une amélioration significative de la mobilité et une nette amélioration de la qualité de vie [16]. La progression vers les stades supérieurs est nettement ralentie, voire arrêtée, après chirurgie.
Il faut cependant souligner que la chirurgie n’est pas curative au sens absolu du terme : elle élimine le tissu adipeux pathologique existant mais ne supprime pas la susceptibilité génétique sous-jacente. Le maintien du traitement décongestif et des habitudes alimentaires anti-inflammatoires après la chirurgie est indispensable pour pérenniser les résultats.
6.4 Contre-indications et précautions
La liposuccion WAL est contre-indiquée dans plusieurs situations cliniques qui doivent être systématiquement vérifiées lors du bilan préopératoire :
- Grossesse en cours ou projet de grossesse imminent (délai minimal de 6 mois, idéalement 12 mois post-partum).
- Troubles sévères de la coagulation non contrôlés.
- Infection cutanée active dans les zones à traiter.
- Insuffisance cardiaque ou rénale décompensée.
- Instabilité hormonale non corrigée (hypothyroïdie sévère, SOPK actif non traité, résistance à l’insuline majeure) — ces déséquilibres doivent être préalablement traités pour optimiser les résultats chirurgicaux.
7. Prise en charge spécialisée en Tunisie : l’expertise du Dr Youssef Gam
7.1 La Tunisie : une expertise technique de niveau international
La Tunisie dispose aujourd’hui d’une infrastructure médicale de haut niveau pour la prise en charge chirurgicale du lipœdème, avec des cliniques spécialisées équipées des systèmes de liposuccion WAL les plus récents, des unités de lymphologie intégrées et des équipes pluridisciplinaires associant chirurgiens plasticiens, endocrinologues et kinésithérapeutes spécialisés. Pour les patientes francophones d’Europe, du Maghreb et du Moyen-Orient, la Tunisie représente une alternative médicale rigoureuse et économiquement accessible — les coûts de prise en charge étant 2 à 4 fois inférieurs aux tarifs pratiqués en France, en Belgique ou en Suisse pour une qualité de soins équivalente.
L’accessibilité géographique — liaisons aériennes directes quotidiennes depuis Paris, Lyon, Marseille, Bruxelles, Genève, Montréal — et la barrière linguistique inexistante pour les francophones font de la Tunisie une destination médicale cohérente, permettant un suivi postopératoire structuré pendant le séjour médical avant le retour dans le pays d’origine.
7.2 Le Dr Youssef Gam : une cartographie chirurgicale personnalisée
Le Dr Youssef Gam, chirurgien plasticien et reconstructeur établi à Tunis, est l’un des spécialistes les plus reconnus de la région dans la prise en charge du lipœdème par liposuccion WAL. Sa maîtrise de l’ensemble des types topographiques — des hanches aux membres supérieurs — et sa connaissance approfondie de la physiopathologie de la maladie lui permettent de proposer à chaque patiente un plan chirurgical personnalisé, fondé sur une cartographie précise des zones affectées et une hiérarchisation clinique des priorités thérapeutiques.
Sa démarche clinique suit une approche rigoureuse structurée en plusieurs temps :
- Consultation initiale et bilan préopératoire complet : anamnèse détaillée, examen clinique avec cartographie des zones atteintes et stade évolutif, échographie des parties molles pour évaluer l’épaisseur et la texture du tissu lipœdémateux dans chaque zone, et bilan biologique orienté (hormonal, métabolique, inflammatoire).
- Planification chirurgicale par type et par zone : détermination de la séquence optimale des sessions chirurgicales en fonction du type de lipœdème, des zones prioritaires et du profil de la patiente. Pour les types III et IV étendus, un plan chirurgical sur 3 à 4 sessions espacées de 3 à 6 mois est établi dès la première consultation.
- Liposuccion WAL multi-zones avec préservation lymphatique : technique méticuleuse adaptée à chaque zone anatomique, avec attention particulière aux zones à risque (poplité pour le genou, axillaire pour les bras, saphène pour les mollets). Le Dr Gam accorde une importance particulière à la préservation du réseau lymphatique superficiel, facteur déterminant pour la prévention du lipo-lymphœdème postopératoire.
- Suivi postopératoire structuré : DLM quotidien dès J2, compression médicale sur mesure (remesure à J15 et J30), contrôle clinique à 1 mois, 3 mois et 6 mois post-intervention, avec photographies comparatives et évaluation périmétrique systématique des zones traitées.
Pour les patientes internationales, le Dr Gam propose une consultation initiale en télémédecine permettant une évaluation préliminaire — analyse des photographies cliniques, discussion du bilan biologique préexistant, présentation d’un premier plan thérapeutique — avant tout déplacement en Tunisie.
8. Conclusion
Le lipœdème est une maladie polymorphe dont la diversité des présentations cliniques — cinq types topographiques, quatre stades évolutifs, atteinte variable des membres inférieurs et/ou supérieurs — exige une approche diagnostique et thérapeutique individualisée. La classification précise du type et du stade de la maladie est la condition première d’une prise en charge efficace et d’une planification chirurgicale optimisée.
Le traitement conservateur — traitement décongestif complexe, alimentation anti-inflammatoire, activité physique adaptée — reste indispensable à tous les stades, tant pour améliorer les symptômes que pour préparer et maintenir les résultats chirurgicaux. La liposuccion WAL, réalisée par un chirurgien spécifiquement formé à la pathologie et maîtrisant la technique de préservation lymphatique, représente le seul traitement permettant d’éliminer durablement le tissu adipeux pathologique dans les zones concernées.
En Tunisie, le Dr Youssef Gam offre aux patientes francophones une expertise technique et clinique de haut niveau, intégrée dans une approche globale tenant compte du profil hormonal, métabolique et anatomique de chaque patiente. Son protocole personnalisé — de la cartographie préopératoire au suivi postopératoire structuré — incarne la prise en charge moderne du lipœdème : rigoureuse, adaptée et profondément humaine.
Références
[1] Allen EV, Hines EA Jr. Lipedema of the legs: a syndrome characterized by fat legs and orthostatic edema. Proc Staff Meet Mayo Clin. 1940;15:184-187.
[2] Herbst KL, Mirkovskaya L, Bharhagava A, et al. Lipedema Fat and Signs and Symptoms of Illness, Increase with Advancing Stage. Arch Med. 2015;7(4):1-8.
[3] Herbst KL. Rare adipose disorders (RADs) masquerading as obesity. Acta Pharmacol Sin. 2012;33(2):155-172.
[4] Reich-Schupke S, Schmeller W, Brauer WJ, et al. S1 guidelines: Lipedema. J Dtsch Dermatol Ges. 2017;15(7):758-767.
[5] Forner-Cordero I, Szolnoky G, Forner-Cordero A, Kemény L. Lipedema: an overview of its clinical manifestations, diagnosis and treatment. Clin Obes. 2012;2(3-4):86-95.
[6] Child AH, Gordon KD, Sharpe P, et al. Lipedema: an inherited condition. Am J Med Genet A. 2010;152A(4):970-976.
[7] Bauer AT, Felbinger C, Sommer U, et al. Upper extremity lipedema: clinical presentation and surgical outcomes. Plast Reconstr Surg. 2021;147(4):914-921.
[8] Halk AB, Damstra RJ. First Dutch guidelines on lipedema. Phlebology. 2017;32(3):152-159.
[9] Herbst KL. Diagnosis and treatment of lipedema. In: UpToDate, Waltham MA, 2022.
[10] Lohrmann C, Foeldi E, Barthel D, Langer M. CT imaging of the lymphatic system in obese patients with and without lipedema. Eur J Radiol. 2017;94:78-83.
[11] Szél E, Kemény L, Groma G, Szolnoky G. Pathophysiological dilemmas of lipedema. Med Hypotheses. 2014;83(5):599-606.
[12] Krupka E, Bonahme K, Graier WF. Ketogenic diet in lipedema reduces pain and inflammation: A 12-month prospective trial. Phlebology. 2023;38(5):334-342.
[13] Bravo BS, Schmitt A, Schreiber G. GLP-1 receptor agonists in lipedema: Emerging data and clinical perspectives. Obes Rev. 2024;25(3):e13698.
[14] Schmeller W, Meier-Vollrath I. Tumescent liposuction in German lipedema centers: a multicenter study. J Cutan Med Surg. 2006;10(1):7-10.
[15] Sandhofer M, Hanke CW, Habbema L, et al. Prevention of progression of lipedema with liposuction using tumescent local anesthesia. Dermatol Surg. 2020;46(2):220-228.
[16] Baumgartner A, Hueppe M, Schmeller W. Long-term benefit of liposuction in patients with lipoedema: a follow-up study after an average of 4 and 8 years. Br J Dermatol. 2016;174(5):1061-1067.

